Diese Seiten befinden sich im Aufbau
Forschungsschwerpunkte
Idiopathische männliche Infertilität
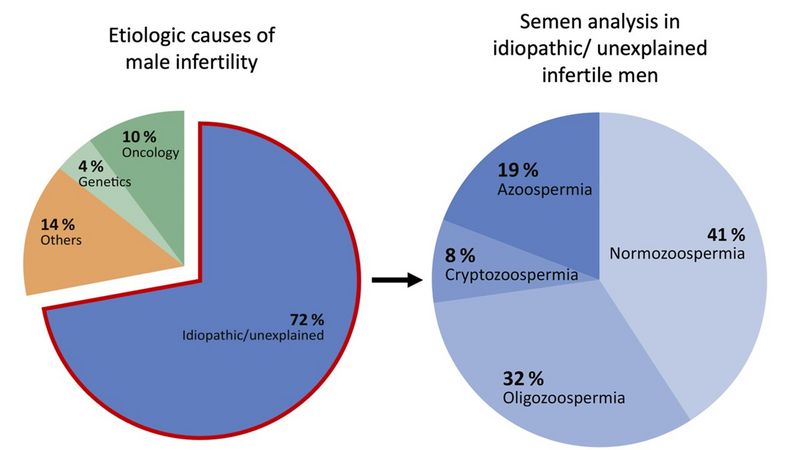
adapted from Tüttelmann et al., 2018 In den westlichen Ländern sind mindestens 15 % der Paare im reproduktiven Alter von Infertilität betroffen, bei 50 % trägt ein männlicher Faktor wesentlich dazu bei. Nicht-genetische Faktoren wie eine hochgradige Varikozele, ein Maldescensus testis in der Anamnese oder die Behandlung onkologischer Erkrankungen können bei einem von vier Patienten die beeinträchtigte Fruchtbarkeit erklären (Abb.). Bei der Mehrheit der infertilen Männer geht man jedoch davon aus, dass genetische Faktoren eine entscheidende Rolle spielen: In diesen Fällen lässt sich die Infertilität im Allgemeinen in eine seltene klassische monogene Form (etwa 4 % der Fälle) und eine viel häufigere (>70 %) multifaktorielle Form (auch als genetisch komplex bezeichnet) einteilen. Letztere ist eine Kombination aus häufigen genetischen Faktoren, Umweltfaktoren und Lebensstil.
Die Infertilität dieser Männer ist derzeit unbekannten Ursprungs und wird als
i) idiopathisch bezeichnet, wenn die Spermienparameter beeinträchtigt sind (z. B. niedrige Spermienzahl - Oligozoospermie), und
ii) ungeklärt, wenn die Samenanalyse normale Spermienparameter aufweist (Normozoospermie) (Schlegel et al., 2021).
Trotz des heterogenen Phänotyps der Gesamtspermienzahl (TSC) bei diesen Männern, ist ihnen das Merkmal der männlichen Infertilität gemeinsam.Das Ziel der Arbeitsgruppe Translationalen Andrologie ist es, durch die Identifizierung weiterer ätiologischer Faktoren die Anzahl der idiopathisch infertilen Männer zu minimieren.
Durch verschiedene Projekte ist uns dies bereits gelungen, hierbei lag der Fokus klar in der Analyse der Bedeutung der Genotypisierung des FSHB Polymorphismus (FSHB c.-211 G>T)in der männlichen Infertilität: In den aktuellen Projekten haben wir mit Techniken wie Genom-weiten Assoziationsstudien (GWAS), histo-pathologischer Aufarbeitung von Hodengewebeproben und eines Clusterings einer großen Patientengruppe (eine Form des Machine Learnings/Artificial Intelligence) die Bedeutung dieses Polymorphismus weiter untersuchen können. Es gelang uns damit den Einfluss von FSHB c.-211 G>T auf das FSH-Serumlevel, die Sertolizellen (Stützzellen) im Hoden und die klinische Bedeutung in der Kinderwunsch-Diagnostik darzustellen.
Weiterführende Literatur
Schwarzkopf V, Wistuba J, Sandhowe-Klaverkamp R, Kliesch S, Gromoll J, Schubert M. Unraveling a subgroup of men with unexplained male infertility - men with normogonadotropic non-obstructive azoospermia. J Clin Endocrinol Metab. 2025 Apr. doi: 10.1210/clinem/dgaf200.
Silva AFN*, Schubert M*, Kliesch S, Schlatt S, Ramalho-Santos J, Amaral SCG. Prevalence and impact of antisperm antibodies on semen quality and male reproductive health aspects: A 10-years retrospective study. Andrology. 2025 Mar 11. doi: 10.1111/andr.70020.
Schubert M*, Pérez Lanuza L*, Wöste M, Dugas M, Carmona FD, Palomino-Morales RJ, Rassam Y, Heilmann-Heimbach S, Tüttelmann F, Kliesch S, Gromoll J. A GWAS in Idiopathic/Unexplained Infertile Men Detects a Genomic Region Determining Follicle-Stimulating Hormone Levels. J Clin Endocrinol Metab. 2022 Jul. doi: 10.1210/clinem/dgac165.
Krenz H, Sansone A, Kliesch S, Gromoll J, Schubert M. FSHB Genotype Identified as a Relevant Diagnostic Parameter Revealed by Cluster Analysis of Men With Idiopathic Infertility. Front Endocrinol (Lausanne). 2021 Dec. doi: 10.3389/fendo.2021.780403.
Schubert M, Kaldewey S, Pérez Lanuza L, Krenz H, Dugas M, Berres S, Kliesch S, Wistuba J, Gromoll J. Does the FSHB c.-211G>T polymorphism impact Sertoli cell number and the spermatogenic potential in infertile patients? Andrology. 2020 Sep. doi: 10.1111/andr.12777.
Infertilität und Komorbiditäten
Die meisten Männer mit Fertilitätsstörungen sind zum Zeitpunkt der Abklärung ansonsten gesund. Dennoch haben zahlreiche Studien wiederholt gezeigt, dass infertile Männer ein erhöhtes Risiko für die Entwicklung von Begleiterkrankungen aufweisen – auch wenn die kausalen Zusammenhänge zwischen diesen Erkrankungen bisher weitgehend unklar bleiben.
Besonders beschrieben wurden Assoziationen zwischen männlicher Infertilität und Komorbiditäten wie Herz-Kreislauf-Erkrankungen (einschließlich erhöhter Sterblichkeit), Bluthochdruck, Typ-2-Diabetes, metabolischem Syndrom, Autoimmunerkrankungen (wie Multiple Sklerose), Keimzelltumoren des Hodens sowie Prostatakrebs.
Viele dieser Studien basieren auf Gesundheitsakten oder Beobachtungsstudien, bei denen die Diagnose „Infertilität“ auf Fragebogendaten oder der Auswertung medizinischer Unterlagen beruht. Infolgedessen fehlt es diesen Untersuchungen häufig an einer tiefgehenden phänotypischen Charakterisierung der Patienten, und sie berücksichtigen nicht die zugrunde liegende Heterogenität der Infertilitätsursachen.
Für einige Formen der Infertilität, wie etwa der sekundäre Hypogonadismus, bei dem ein erniedrigter Testosteronspiegel als Risikofaktor für spätere Komorbiditäten gelten kann, ist der kausale Zusammenhang offensichtlich.
Bei der Mehrheit der infertilen Männer lässt sich jedoch bisher keine eindeutige Ursache feststellen. Die männliche Infertilität unbekannter Ätiologie – d. h. idiopathische (bei auffälligen Spermienparametern) oder ungeklärte Infertilität (bei unauffälligen Spermienparametern) – wird wahrscheinlich durch eine Kombination häufiger genetischer, umweltbedingter und lebensstilabhängiger Faktoren verursacht.
Das Zusammenspiel dieser Faktoren ist bislang jedoch unzureichend erforscht. Dadurch ist die diagnostische Genauigkeit eingeschränkt, was zu einem hohen Anteil pathomechanistisch ungeklärter Infertilität führt – und personalisierte Medizin sowie die Identifikation möglicher gemeinsamer ätiologischer Grundlagen von Infertilität und Begleiterkrankungen erheblich erschwert.
In der Arbeitsgruppe nähern wir uns diesem Thema über zwei Projekte:
- In einer Kooperation mit Prof. Dr. André Karch, (s. Kooperationen und Grants), Prof. Dr. Sabine Kliesch, Mattia Anfosso und Frau Dr. Simone Bier führen wir eine Re-Evaluation von infertilen Männern durch und fokussieren dabei auf die Veränderungen der andrologischen Parameter im Lauf der Jahre und auf die möglicherweise neu entwickelten Komorbiditäten. In diesem Projekt werden frühere Patienten rekontaktiert und erneut einbestellt. Die Daten werden perspektivisch mit den epidemiologischen Daten der NAKO (Nationale Kohorte) abgeglichen.
- Männliche Infertilität unbekannter Ätiologie – also idiopathische oder ungeklärte Infertilität – wird wahrscheinlich durch eine Kombination häufiger genetischer, umweltbedingter und lebensstilabhängiger Faktoren verursacht. In diesem Zusammenhang haben Genomweite Assoziationsstudien (GWAS) das Potenzial, maßgeblich zur Identifizierung neuer genetischer Risikofaktoren für männliche Infertilität und verwandte Merkmale beizutragen. So konnten wir in früheren Arbeiten zeigen, dass bestimmte Einzelnukleotid-Polymorphismen (SNPs) die Konzentration des Follikel-stimulierenden Hormons (FSH) beeinflussen und damit zur zugrunde liegenden Ätiologie beitragen.
In einem Kooperationsprojekt mit Prof. Dr. Christina Lill und Dr. Olena Ohlei (S.Kooperationspartner und Grants) wollen wir neue Kandidaten-SNPs gemeinsam mit den bereits beschriebenen FSH-assoziierten SNPs identifizieren, um ein Panel genetischer Risikofaktoren für idiopathische und ungeklärte männliche Infertilität zu entwickeln. Dies könnte den Weg für eine verbesserte Phänotypisierung ebnen und damit die Diagnostik im Rahmen der Fertilitätsabklärung bei Männern entscheidend voranbringen.
Wissen, Erfahrungen und Entscheidungen im Kontext der andrologischen Diagnostik und Therapie(empfehlungen) bei männlicher Infertilität
Der diagnostische und therapeutische Prozess bei unerfülltem Kinderwunsch stellt eine besondere Herausforderung für Paare dar. Vor allem die Erfahrungen, die Männer dabei machen, sind bislang wenig erforscht – insbesondere dann, wenn die Ursache für das Ausbleiben einer Schwangerschaft möglichweise auf der männlichen Seite liegt. Mit unserer Studie möchten wir dies ändern.
In einem Kooperationsprojekt mit Dr. Markus Kluge (S. Kooperationspartner) interessiert uns, wie Männer den Diagnose- und beginnenden Therapieprozess bei unerfülltem Kinderwunsch erleben, welche Herausforderungen sie erfahren und welche Entscheidungen sie für sich (und gemeinsam mit ihrer Partnerin) treffen. Dabei wollen wir vor allem verstehen, welche Bedeutung dabei außerklinische Medien, Informationsquellen und Wissensbestände spielen.
Im Rahmen der Studie werden drei Interviews von jeweils ca. 45 Minuten durchgeführt.

