Zelluläre Mikrobiologie
Unsere Arbeitsgruppe arbeitet an verschiedenen Aspekten der Pathogenese von Staphylococcus aureus. Dieser Keim ist ein häufig harmloser Besiedler der Haut und Schleimhäute, kann aber auch eine pathogene Bedeutung erlangen. Er ist ein extrem vielseitiger Erreger und kann schwere Infektionen wie Endokarditis, Osteomyelitis und Lungenentzündung hervorrufen.
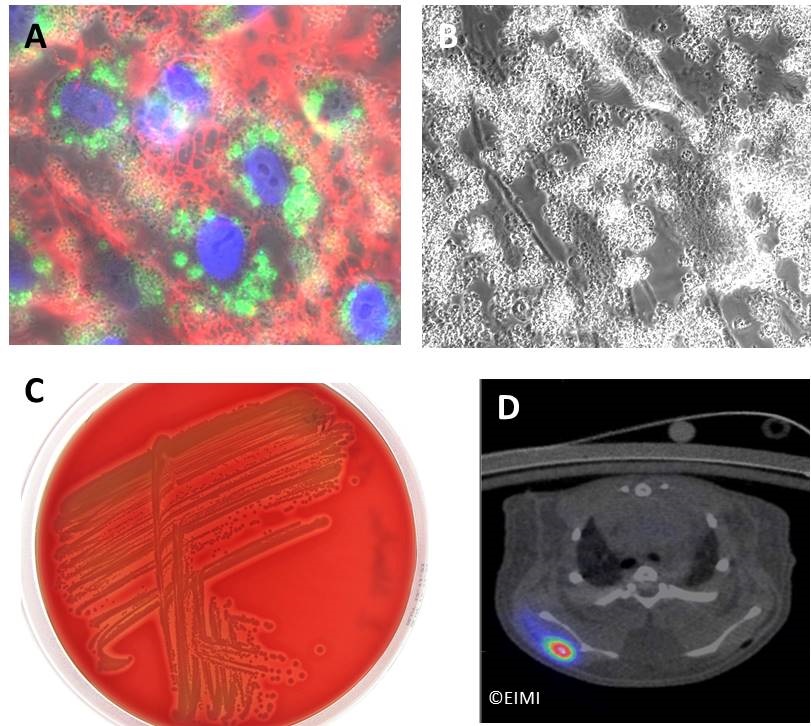
Seit einigen Jahren ist bekannt, dass S.aureus in Wirtszellen wie Epithel- und Endothelzellen und Osteoblasten eindringen kann, wo der Erreger einerseits geschützt ist vor dem Immunsystem, andererseits aber auch die Zellen von innen heraus zerstören, und durch die Zellen hindurch in tiefer gelegene Gewebeschichten eindringen kann. Wir interessieren uns für die bakteriellen als auch die Wirtszellfaktoren, die die Invasion der Zellen ermöglichen oder aber auch blockieren.
In einem gemeinsamen Projekt mit der AG Schaumburg untersuchen wir die Pathogenität von S.schweitzeri, der häufig in afrikanischen Fledermäusen und Affen vorkommt, aber (bisher) nur selten auf den Menschen übertragen wird.
In Zusammenarbeit mit dem Europäischen Institut für Molekulare Bildgebung (EIMI) beschäftigen wir uns mit der Frage, wie lebensbedrohliche bakterielle Infektionen nicht -invasiv in vivo sichtbar gemacht werden können. Zu diesem Zeitpunkt entwickeln und validieren wir spezifische bildgebende Sonden, die auf einer selektiven Stoffwechselaufnahme der Bakterien basieren. (Link)

