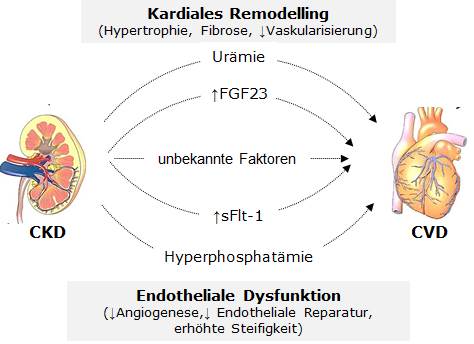
Chronische Nierenerkrankungen (CKD) sind ein weltweit verbreitetes Krankheitsbild und stellen einen Risikofaktor für das Auftreten von kardiovaskulären Erkrankungen (CVD) dar. Es ist bekannt, dass die CKD sowohl beim Menschen als auch in verschiedenen Tiermodellen zu strukturellen und funktionellen kardialen Veränderungen führt. Diese kardialen Veränderungen (sog. kardiales Remodelling) sind u.a. charakterisiert durch die Entwicklung einer Bluthochdruckerkrankung, eine reduzierte myokardiale Vaskularisierung bzw. eine mikrovaskuläre Dysfunktion und eine interstitielle Fibrose.
Sogenannte "klassische" kardiovaskuläre Risikofaktoren wie z.B. das Alter, Diabetes und/oder Bluthochdruck triggern das erhöhte kardiovaskuläre Risiko von CKD-Patienten. Daneben gibt es wahrscheinlich noch zahlreiche weitere bisher unbekannte Risikofaktoren, die das kardiovaskuläre Risiko von nierenerkrankten Patienten erhöhen. Dazu zählen u.a. urämische Toxine, die Aktivierung des Renin-Angiotensin-Systems, verminderte Hämoglobinwerte, eine Mikroalbminurie, erhöhte Entzündungswerte, oxidativer Stress und andere Faktoren.
Die Untersuchung und Identifizierung bisher unbekannter CKD assoziierter Mechanismen, die das kardiovaskuläre Risiko von nierenerkrankten Patienten beeinflussen wird es in Zukunft möglicherweise ermöglichen, neue Therapiekonzepte für CKD Patienten zu entwickeln.
Aktuell stehen zwei Forschungsgebiete im zentralen Fokus unserer Arbeitsgruppe:
- CKD-assoziiertes kardiales Remodelling
- CKD-assoziierte endotheliale Dysfunktion und Störungen in der (myokardialen) Angiogenese

