Arbeitsgruppe Schwab
Wir arbeiten an der Schnittstelle zwischen Grundlagenforschung und angewandter, translationaler Forschung. In den meisten Fällen heißt dies, dass wir humane Biomaterialien (nicht benötigte Blutspende-Abfallprodukte, Biopsiegewebe, etc) entweder direkt analysieren oder diese in unseren experimentellen in vitro-Systemen einsetzen. Besondere Krankheitsschwerpunkte sind Multiple Sklerose (MS), Rasmussen Enzephalitis (RE), und Progressive Multifokale Leukenzephalopathie (PML) und wir interessieren uns in diesem Zusammenhang besonders für die Blut-Hirn-Schranken-Migration von Immunzellen, T-Zell-Rezeptor-Analysen, Biomarkerforschung, und die Immunkontrolle von viralen Infektionen.
Einige unserer derzeitigen konkreten Forschungsprojekte sind im Folgenden gelistet:
Die Migration von T-Lymphozyten über die (nicht) entzündete Blut-Hirn-Schranke
In neuro-inflammatorischen Erkrankungen wie z.B. der MS wandern Immunzellen über das entzündete Endothel der Blut-Hirn-Schranke und erzeugen dann im zentralen Nervensystem (ZNS) Schäden, die zu den bekannten Krankheitssymptomen führen. Dieses Wissen hat dazu geführt, dass die Hemmung der Migration über das Endothel eine wirksame Behandlungsstrategie im Bereich der MS wurde in der Form von Medikamenten wie z.B. Natalizumab. Wir erforschen daher die genauen Mechanismen, wie Immunzellen diese Wanderung ins ZNS bewerkstelligen und wie man sie potentiell beeinflussen kann.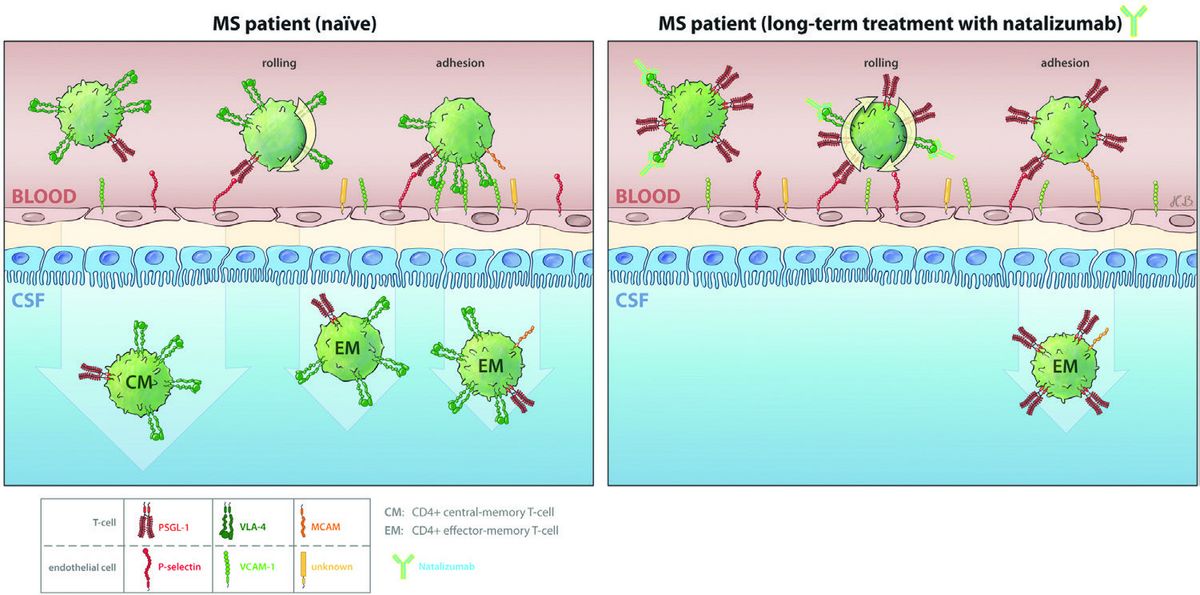
Schwab et al., 2014 Validierung von / Forschung am Biomarker L-Selektin für PML-Risikostratifizierung
Wir haben 2013 den Biomarker L-Selektin entdeckt, der das Risiko von Natalizumab-behandelten Patienten eingrenzen kann, an einer PML zu erkranken. Seither forschen wir an den biologischen Zusammenhängen des Moleküls mit der Entwicklung der Erkrankung. Die PML wird von einem Virus ausgelöst wird, mit dem die meisten Menschen lebenslang infiziert sind, das John-Cunningham-Virus (JC-Virus), ohne dass dies zu einer Pathologie führt; außerdem sammeln wir prospektiv Daten von Patienten im Rahmen einer longitudinalen Validierung des Biomarkers.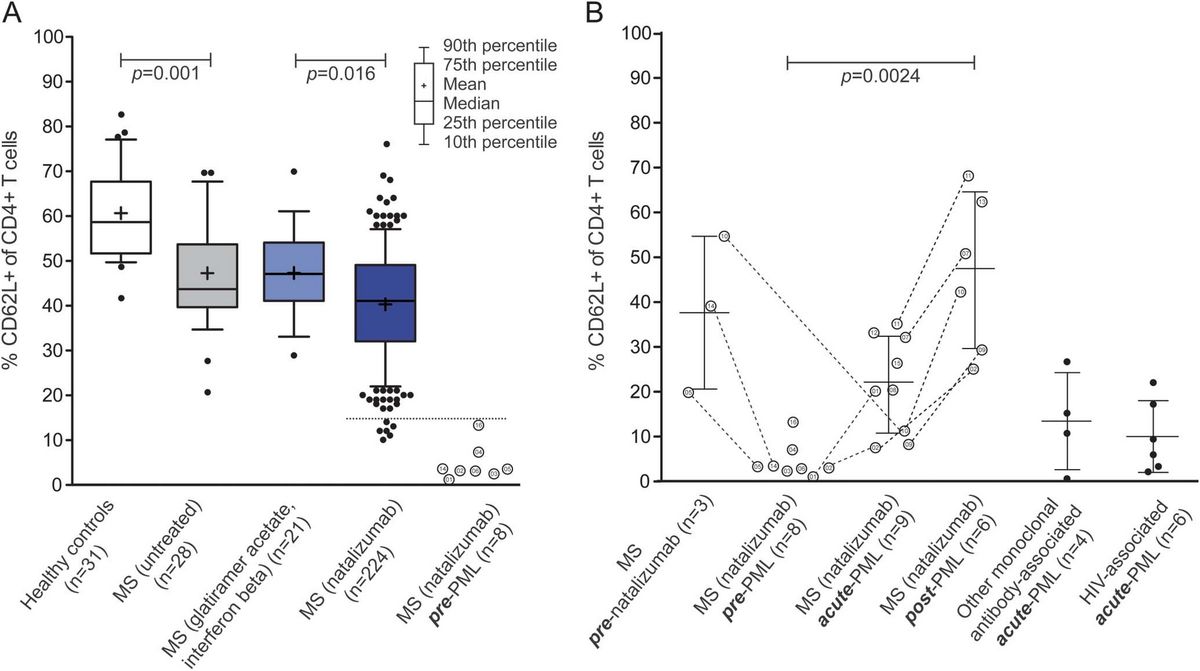
Schwab et al. 2013 Die adaptive zelluläre Immunantwort gegen das John-Cunningham-Virus
Das JC-Virus ist verantwortlich für die PML und wir interessieren uns in diesem Zusammenhang für die spezifische T-Zell-Antwort auf die lebenslange Infektion mit diesem Virus. Wir versuchen herauszufinden, wie das gesunde Immunsystem das Virus unter Kontrolle hält, aber auch was passiert, wenn immungeschädigte Menschen einen Ausbruch der Infektion nicht mehr verhindern können.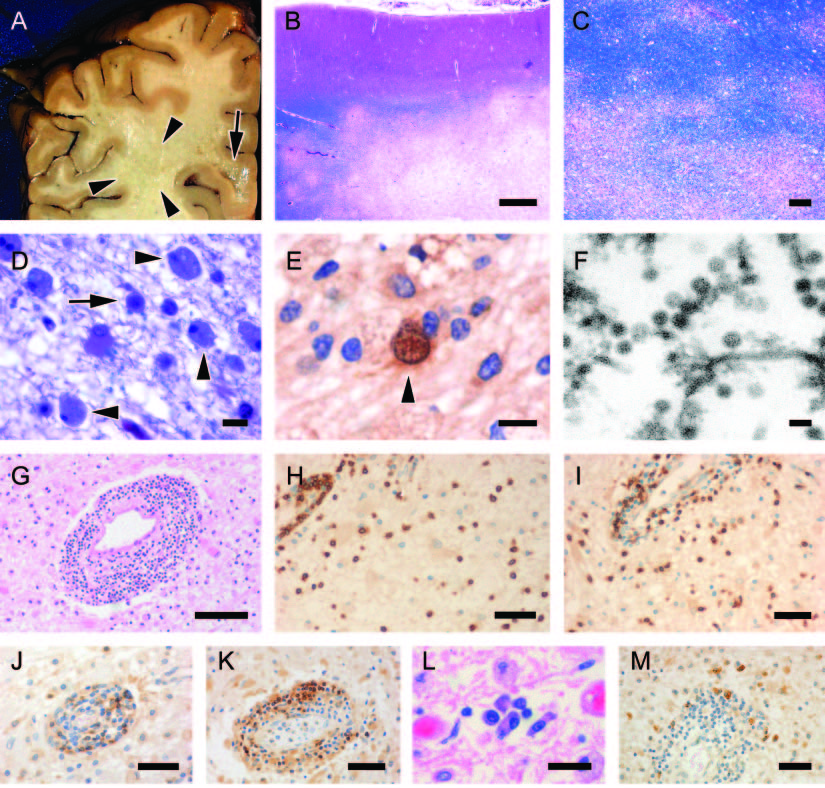
Schwab et al., 2012 Der Einfluss von Umweltfaktoren über die Haut auf die zentralnervöse Immunantwort
Es ist seit langem bekannt, dass in Regionen mit hoher Sonneneinstrahlung die Immunantwort anders verläuft, z.B. gibt es dort weniger MS. Auch haben MS-Patienten im Sommer weniger Schübe und Kinder, die im Winter geboren werden / deren Mütter mit ihnen im Sommer schwanger waren, entwickeln seltener MS. Wir untersuchen zusammen mit der Dermatologie des UKM, welche molekularen Mechanismen hier eine Rolle spielen. Im Idealfall wollen wir dabei helfen, Medikamente zu entwickeln, die die Umwelt imitieren können, um somit die Krankheitsschwere der MS oder ihre Entstehung positiv beeinflussen zu können.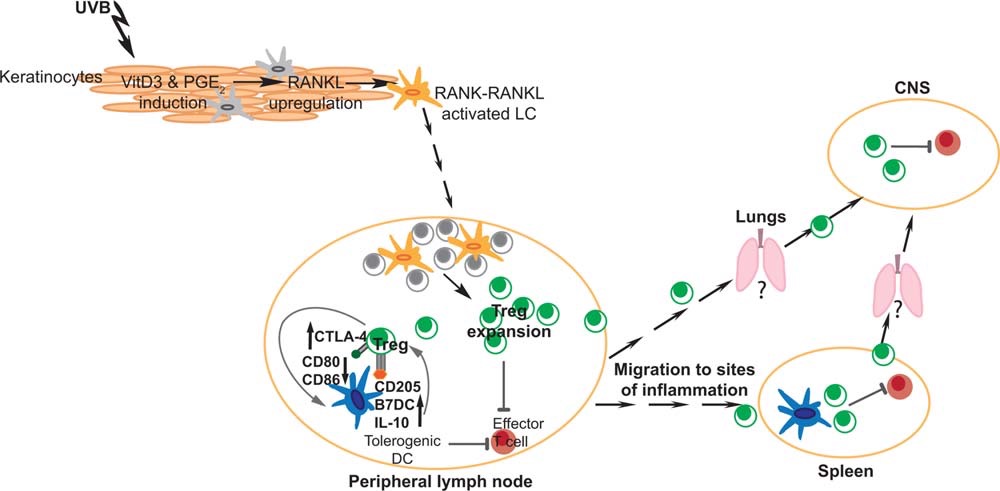
Breuer et al. 2014 Die T-Zell-vermittelte Pathologie der Rasmussen-Enzephalitis
Die RE ist eine pädiatrische Epilepsie und bekannt für ihren Ursprung im Immunsystem. Wir sind seit vielen Jahren an der Ätiologie der Erkrankung interessiert und versuchen gegenwärtig zu verstehen, weshalb CD8+ T-Zellen in diesen Patienten die ZNS-Strukturen angreifen und ob man Anzeichen dieses Angriffs im Blut der Patienten genau genug nachweisen kann, um es als diagnostische Hilfe nutzen zu können.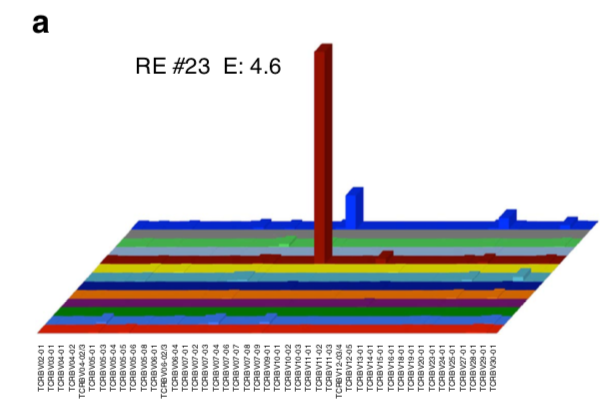
Schneider-Hohendorf et al., 2016
Ausgewählte Publikationen
Förderung
Kooperationen
- Dr. med. Kornelius Kerl, Klinik für Kinder- und Jugendmedizin - Pädiatrische Hämatologie und Onkologie
- Prof. Dr. rer. nat. Karin Loser, Klinik für Hautkrankheuten, AG Experimentelle Dermatologie und Immunbiologie der Haut
- PD Dr. med. Astrid Jeibmann, Institut für Neuropathologie
- Prof. Dr. med. Tanja Kuhlmann, Institut für Neuropathologie
- PD Dr. med. Judith Alferink, Klinik für Psychatrie und Psychotherapie , AG Molekulare Immunologie psychiatrischer Erkrankungen
- Univ.-Prof. Dr. rer. nat. Lydia Sorokin, Institut für Physiologische Chemie und Pathobiochemie
- Univ.-Prof. Dr. rer. nat. Ulrich Dobrindt, Institut für Hygiene, AG Mikrobielle Genomplastizität
- Univ.-Prof. Dr. med. Alexander Zarbock, Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie
- Prof. Dr. med. Thomas Korn, Neurologische Universitätsklinik der Technischen Universität München
- PD Dr. rer. nat. Klaus Dornmair, Institut für klinische Neuroimmunologie der Ludwig-Maximilian-Universität München
- David Brassat, MD, PhD, Centre Hospitalier Universitaire de Toulouse
- Hans H. Hirsch, Universitätsspital Basel, Department Biomedizin
- Dr. rer. nat. Jean-Luc Murk, Elisabeth-Tweesteden Hospital Tilburg, Laboratory for Medical Microbiology and Immunology
- PD Dr. med. Chi-Wang Ip, Neurologische Klinik des Universitätsklinikums Würzburg
- Prof. Dr. rer. nat. Manfred Lutz, Institut für Virologie und Immunbiologie der Universität Würzburg

